СЗМБ
Предтрансплантационная диагностика
Диагностика донора и реципиента перед органной трансплантацией заключается в иммунологическом обследовании пациентов для предупреждения отторжения трансплантата. Реакция отторжения — определяется иммунным ответом реципиента на чужеродные антигены. Ключевыми антигенами, которые стимулируют отторжение аллогенного трансплантата, являются молекулы закодированные главным комплексом гистосовместимости (ГКГС, англ. Major histocompatibility complex – МНС). У человека эти антигены называются HLA (от англ. human leukocyte antigens), в связи с тем, что они выявляются на лимфоцитах и других лейкоцитах периферической крови. Антигены гистосовместимости (трансплантационные антигены) экспрессируются на всех ядросодержащих клетках и тромбоцитах. У человека наибольшее их количество содержится в лимфоидной ткани (на лимфоцитах и макрофагах).
Ключевую роль в успешном исходе трансплантации играет степень биологической совместимости донора и реципиента по HLA антигенам, а так же идентификации предсуществующих антител реципиента к антигенам донора.
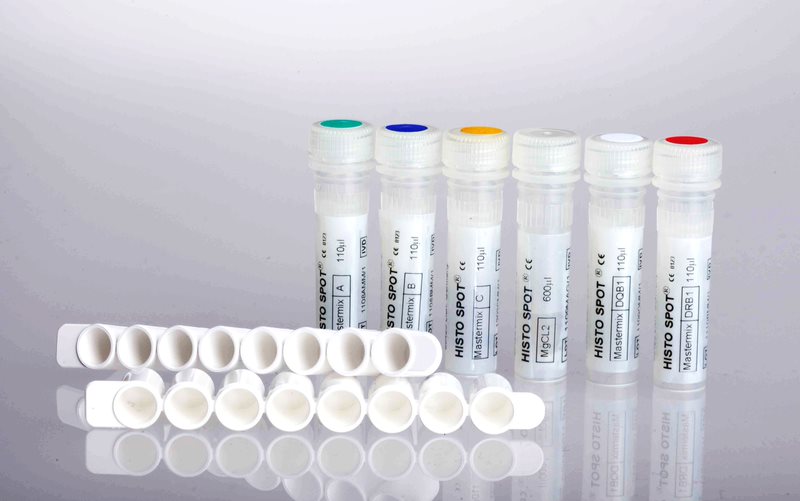
Система HISTO SPOT SSO производства BAG DIAGNOSTICS
— представляет собой тест для in vitro диагностики и помогает проводить гистотипирование HLA аллелей на молекулярно-генетической основе. Гистотипирование HLA позволяет получать результаты в диапазоне от низкого до среднего разрешения.
Система HISTO SPOT ® SSO основана на гибридизации амплифицированной ДНК со специфическими для последовательности олигонуклеотидами.
Автоматизированный рабочий процесс включает в себя следующие решения:
— Наборы HISTO SPOT® (гистотипирование локусов HLA — A, B, C, DRB1, DQB1);
— Наборы HISTO SPOT® HLA AB (скрининг и идентификация антител)
— MR.SPOT® Процессор;
— Программное обеспечение HISTOMATCH.
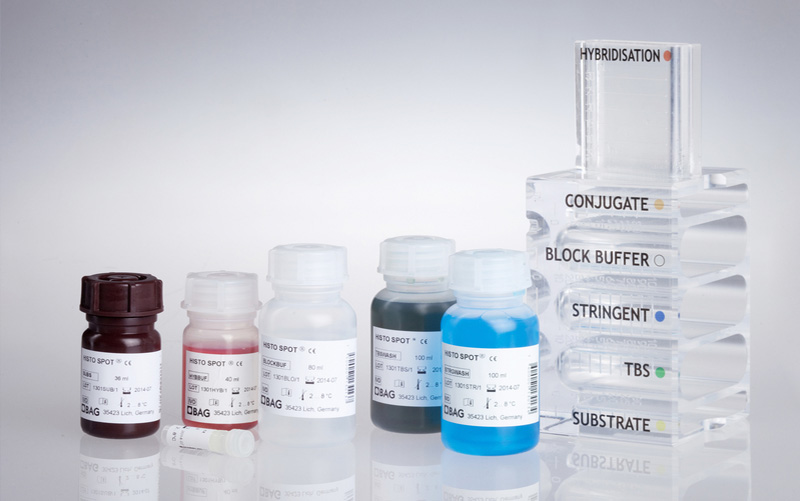
Система HISTO SPOT® HLA AB – тест для in vitro диагностики предсуществующих антител к лейкоцитарным антигенам. Программное обеспечение HISTO MATCH совместно с процессором mr. SPOT – вариант высокого уровня автоматизации вместо сложного рутинного анализа. Использование микроматрицы с рекомбинантными аллель-специфическими белками дает результаты с высоким разрешением и не требует ручных вмешательств специалиста. Прямая идентификация HLA-антител благодаря рекомбинантным одиночным антигенам для HLA класса I и HLA класса II с использованием минимального объема образца (2-10 мкл сыворотки). Пропускная способность от 1 до 96 образцов.

Процессор MR.SPOT® и Программное обеспечение HISTOMATCH
Процессор MR.SPOT ® гарантирует высокую точность и быстрые результаты при малых объемах и высокой производительности.
На приборе можно обрабатывать от 1 до 96 тестов за один запуск, до трех запусков в день. Благодаря высокой степени автоматизации и малому времени ручного труда система также идеально подходит для работы в ночную смену.
MR.SPOT ® автономно выполняет весь анализ от ампликона до результата. Полностью автоматическая промывка и пипетирование делают устройство очень простым в использовании. Для документирования процесса MR.SPOT ® автоматически записывает все результаты с помощью встроенной камеры и передает изображение в программу HISTO MATCH для удобной оценки. SQL server – база данных, хранящая все данные по исследованиям во избежание потери/удаления/сбоев при прогоне протокола.
MR.SPOT ® позволяет считывать штрих-коды для всех комплектов реагентов и измерять объемы расходных реактивов в соответствии с количеством исследуемых образцов. Коммерчески доступные системы могут быть интегрированы в рабочий процесс для выделения ДНК и настройки ПЦР.
Все системы и расходные материалы для проведения гистотипирования имеют регистрационное удостоверение. (здесь вложим кликабельные сертификаты)
Подтверждающая методика типирования:
— Гистотипирование методом SSP (sequence-specific primer) HISTO TYPE SSP – подтверждающая методика типирования для анализа малых объемов образцов. Метод основан на проведении ПЦР с последующей детекцией в форезном геле. Интерпретация результатов SSP возможна в программном обеспечении HISTO MATCH, по завершению внесения полученных результатов электрофореза, программа выдает конечный протокол в pdf формате.
Набор KIR TYPE SSP позволяет провести генотипирование 14 генов иммуноглобулиноподобных рецепторов киллеров (KIR) плюс 2 псевдогена. Это дает дополнительную информацию о возможных различиях между KIR и соответствующими лигандами HLA в контексте трансплантации.
— гистотипирование методом ПЦР в режиме реального времени HISTO TIPE Raynbow — быстрый вариант для типирования 11 локусов в одной пробирке, мультиплексная ПЦР для получения результата менее чем за 80 минут с момента запуска амплификации. Каждая из 96 лунок содержит 1 внутренний контроль амплификации и до 4 специфических реакций аллельных групп в 4 различных каналах. Это увеличивает способность к 384 HLA-специфическим реакциям. Для простой идентификации мы предлагаем программное обеспечение PlexTyper, совместимое с тремя видами амплификаторов:
— CFX (Bio-Rad)
— LightCycler® 480 II
— QuantStudio™ 6 Flex
Молекулярно-генетическая диагностика HLA-ассоциированных заболеваний
Взаимосвязь между определенными типами HLA и некоторыми заболеваниями была подтверждена для более чем 40 различных комбинаций.
Наиболее важной является взаимосвязь HLA-B27 с картиной серонегативного артрита (болезнь Бехтерева, болезнь Рейтера, реактивный артрит). Положительный результат HLA-B27 связан с чрезвычайно высоким риском заболевания (см. Таблицу 1). Чаще всего подтвержденный результат HLA-B27 диагностики вносит значительный вклад в терапию пациента в неясных случаях заболевания с подозрением на болезнь Бехтерева.
|
Заболевания |
Частота B27 у пациентов |
Относительный риск |
|
Анкилозирующий спондилоартрит (Болезнь Бехтерева) |
90.2 % |
91 |
|
Болезнь Рейтера |
78.8 % |
37.6 |
|
Постинфекционный реактивный артрит |
70.2 % |
|
Таблица 1: Частота HLA-B27 и риски.
Пациенты с целиакией не могут принимать в пищу продукты, содержащие глютен, который входит в состав пшеницы, ржи, ячменя и других зерновых. У людей с целиакией глютен вызывает аутоиммунную реакцию, которая приводит к разрушению ворсинок в тонкой кишке. У пациентов формируются антитела, которые атакуют кишечник, вызывая его поражение и патологические изменения. При этом также наблюдается изменение общего состояния организма, например усталость, дефицит питательных веществ. Начало заболевания основывается на двух компонентах: генетическая предрасположенность и некий пусковой механизм. Пусковой механизм может быть внешним (например, рост потребления пшеницы), ситуационным (тяжелый стресс), физическим (беременности, операции) или патологическим (вирусная инфекция).
По причине явной тенденции к семейному распространению целиакии (у 5-10% родственников первого уровня (родители, дети и родные братья) пациентов с диагностированной целиакией также может формироваться целиакия), для раннего начала лечения важна быстрая и надежная диагностика.
Как уже упоминалось ранее, целиакия возникает только у лиц с генетической предрасположенностью. Генетическое наследование целиакии связано с HLA-DQA1*05-DQB1*02 (HLA-DQ2) и HLA-DQA1*03-DQB1*0302 (HLA-DQ8). Эти аллели служат основой для аутоантител целиакии.
Более 90% людей, страдающих от целиакии, имеют одну из этих аллелей, DQ2 или DQ8 (вместо 25% в общей популяции).
Таким образом, молекулярно-генетическое обнаружение генотипов HLA-DQ2 или HLA-DQ8 является чрезвычайно полезным инструментом в диагностике целиакии.
В том случае, когда у пациента с нарушением работы желудочно-кишечного тракта нет маркера DQ2 или DQ8, у него можно практически полностью исключить целиакию.
Новости
Российский Диагностический Саммит 2024
2-4 октября 2024 года в павильоне Крокус Экспо (г. Москва) прошел Четвёртый Российский...
XII Всероссийский съезд трансплантологов
30 сентября – 2 октября 2024 года в городе Москва в НМИЦ трансплантологии и искусственных органов...
Всероссийская конференция «Архитектура донорства: устойчивое развитие, ответственное управление, системное сотрудничество»
11-12 июля в городе Калининград состоялось торжественное открытие Всероссийской конференции...


